Soal Ke-1 Tentang Termodinamika
SOAL KE-1
SOAL TENTANG TERMODINAMIKA
1.) 1,5 m3 gas helium yang bersuhu 27oC dipanaskan secara isobarik sampai 87oC. Jika tekanan gas helium 2 x 105 N/m2 , gas helium melakukan usaha luar sebesar….
A. 60 kJ
B. 120 kJ
C. 280 kJ
D. 480 kJ
E. 660 kJ
Mencari V2 :
V2/T2 = V1/T1
V2 = ( V1/T1 ) x T2 = ( 1,5/300 ) x 360 = 1,8 m3
W = PΔV = 2 x 105(1,8 − 1,5) = 0,6 x 105 = 60 x 103 = 60 kJ
η = ( 1 − Tr / Tt ) x 100
%
Hilangkan saja 100% untuk memudahkan perhitungan :
η = ( 1 − 400/600) = 1/3
η = ( W / Q1 )
1/3 = W/600
W = 200 J
WAC = WAB + WBC
WAC = 0 + (2 x 105)(3,5 − 1,5) = 4 x 105 = 400 kJ
Tt = 640 K
Tr = 240 K (dari hasil perhitungan pertama)
η = ( 1 − Tr/Tt) x 100%
η = ( 1 − 240/640) x 100%
η = ( 5 / 8 ) x 100% = 62,5%
W = Usaha (kerja) = Luas kurva siklus = Luas bidang abcda
W = ab x bc
W = 2 x (2 x 105) = 400 kilojoule
6.) Sebuah mesin Carnot yang menggunakan reservoir suhu tinggi bersuhu 800 K mempunyai efisiensi sebesar 40%. Agar efisiensinya naik menjadi 50%, maka suhu reservoir suhu tinggi dinaikkan menjadi....(UMPTN 90)
A. 900 K
B. 960 K
C. 1000 K
D. 1180 K
E. 1600 K
Pembahasan
Rumus efisiensi (tanpa %)

Data dari Efisiensi pertama,
Tt = 800 K
η = 40% = 0,4 → (1 − η) = 0,6
Dari sini diperoleh suhu rendah Tr

Dari data efisiensi kedua,
η = 50% = 0,5 → (1 − η) = 0,5
Tr = 480 K
Suhu tingginya:

7.) Sejumlah gas ideal mengalami proses seperti gambar berikut.

Proses yang menggambarkan adiabatis dan isokhorik berturut-turut ditunjukkan pada nomor...(UN Fisika 2013)
A. 1 – 2 dan 3 – 4
B. 1 – 2 dan 4 – 5
C. 2 – 3 dan 1 – 2
D. 2 – 3 dan 1 – 2
E. 2 – 3 dan 3 – 4
Pembahasan
Adiabatis : proses dimana tidak ada kalor masuk atau keluar. Ciri garisnya melengkung curam. Seperti garis 2 - 3.
Isokhorik : proses pada volume tetap. Garisnya yang tegak lurus sumbu V. Bisa 5 - 1, juga 3 - 4.
Pilihan yang ada sesuai adiabatis dan isokhoris adalah 2 - 3 dan 3 - 4.
9.)Suatu gas memiliki volume awal 2,0 m3 dipanaskan dengan kondisi isobaris hingga volume akhirnya menjadi 4,5 m3. Jika tekanan gas adalah 2 atm, tentukan usaha luar gas tersebut!
(1 atm = 1,01 x 105 Pa)
SOAL TENTANG TERMODINAMIKA
1.) 1,5 m3 gas helium yang bersuhu 27oC dipanaskan secara isobarik sampai 87oC. Jika tekanan gas helium 2 x 105 N/m2 , gas helium melakukan usaha luar sebesar….
A. 60 kJ
B. 120 kJ
C. 280 kJ
D. 480 kJ
E. 660 kJ
Pembahasan
Data :
V1 = 1,5 m3
T1 = 27oC = 300 K
T2 = 87oC = 360 K
P = 2 x 105 N/m2
W = PΔVData :
V1 = 1,5 m3
T1 = 27oC = 300 K
T2 = 87oC = 360 K
P = 2 x 105 N/m2
Mencari V2 :
V2/T2 = V1/T1
V2 = ( V1/T1 ) x T2 = ( 1,5/300 ) x 360 = 1,8 m3
W = PΔV = 2 x 105(1,8 − 1,5) = 0,6 x 105 = 60 x 103 = 60 kJ
2.) Mesin Carnot bekerja pada suhu tinggi 600 K, untuk menghasilkan kerja mekanik.
Jika mesin menyerap kalor 600 J dengan suhu rendah 400 K, maka usaha yang
dihasilkan adalah….
A. 120 J
B. 124 J
C. 135 J
D. 148 J
E. 200 J
Pembahasan A. 120 J
B. 124 J
C. 135 J
D. 148 J
E. 200 J
Hilangkan saja 100% untuk memudahkan perhitungan :
η = ( 1 − 400/600) = 1/3
η = ( W / Q1 )
1/3 = W/600
W = 200 J
3.) Diagram P−V dari gas helium yang mengalami proses termodinamika ditunjukkan
seperti gambar berikut!
Usaha yang dilakukan gas helium pada proses ABC sebesar….
A. 660 kJ
B. 400 kJ
C. 280 kJ
D. 120 kJ
E. 60 kJ
PembahasanA. 660 kJ
B. 400 kJ
C. 280 kJ
D. 120 kJ
E. 60 kJ
WAC = WAB + WBC
WAC = 0 + (2 x 105)(3,5 − 1,5) = 4 x 105 = 400 kJ
4.) Suatu mesin Carnot, jika reservoir panasnya bersuhu 400 K akan mempunyai
efisiensi 40%. Jika reservoir panasnya bersuhu 640 K, efisiensinya…..%
A. 50,0
B. 52,5
C. 57,0
D. 62,5
E. 64,0
A. 50,0
B. 52,5
C. 57,0
D. 62,5
E. 64,0
Pembahasan
Data pertama:
η = 40% = 4 / 10
Tt = 400 K
Cari terlebih dahulu suhu rendahnya (Tr) hilangkan 100 % untuk mempermudah perhitungan:
η = 1 − (Tr/Tt)
4 / 10 = 1 − (Tr/400)
(Tr/400) = 6 / 10
Tr = 240 K
Data kedua :Data pertama:
η = 40% = 4 / 10
Tt = 400 K
Cari terlebih dahulu suhu rendahnya (Tr) hilangkan 100 % untuk mempermudah perhitungan:
η = 1 − (Tr/Tt)
4 / 10 = 1 − (Tr/400)
(Tr/400) = 6 / 10
Tr = 240 K
Tt = 640 K
Tr = 240 K (dari hasil perhitungan pertama)
η = ( 1 − Tr/Tt) x 100%
η = ( 1 − 240/640) x 100%
η = ( 5 / 8 ) x 100% = 62,5%
5.) Suatu gas ideal mengalami proses siklus seperti pada gambar P −
V di atas. Kerja yang dihasilkan pada proses siklus ini adalah….......kilojoule.
A. 200
B. 400
C. 600
D. 800
E. 1000
PembahasanA. 200
B. 400
C. 600
D. 800
E. 1000
W = Usaha (kerja) = Luas kurva siklus = Luas bidang abcda
W = ab x bc
W = 2 x (2 x 105) = 400 kilojoule
6.) Sebuah mesin Carnot yang menggunakan reservoir suhu tinggi bersuhu 800 K mempunyai efisiensi sebesar 40%. Agar efisiensinya naik menjadi 50%, maka suhu reservoir suhu tinggi dinaikkan menjadi....(UMPTN 90)
A. 900 K
B. 960 K
C. 1000 K
D. 1180 K
E. 1600 K
Pembahasan
Rumus efisiensi (tanpa %)
Data dari Efisiensi pertama,
Tt = 800 K
η = 40% = 0,4 → (1 − η) = 0,6
Dari sini diperoleh suhu rendah Tr
Dari data efisiensi kedua,
η = 50% = 0,5 → (1 − η) = 0,5
Tr = 480 K
Suhu tingginya:
7.) Sejumlah gas ideal mengalami proses seperti gambar berikut.
Proses yang menggambarkan adiabatis dan isokhorik berturut-turut ditunjukkan pada nomor...(UN Fisika 2013)
A. 1 – 2 dan 3 – 4
B. 1 – 2 dan 4 – 5
C. 2 – 3 dan 1 – 2
D. 2 – 3 dan 1 – 2
E. 2 – 3 dan 3 – 4
Pembahasan
Adiabatis : proses dimana tidak ada kalor masuk atau keluar. Ciri garisnya melengkung curam. Seperti garis 2 - 3.
Isokhorik : proses pada volume tetap. Garisnya yang tegak lurus sumbu V. Bisa 5 - 1, juga 3 - 4.
Pilihan yang ada sesuai adiabatis dan isokhoris adalah 2 - 3 dan 3 - 4.
8.) Perhatikan
gambar! Gas ideal melakukan proses perubahan tekanan (P) terhadap
volume (V). Usaha yang dilakukan oleh gas pada proses tersebut adalah…
A. 20 Joule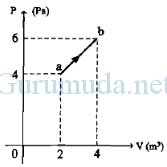

B. 15 Joule
C. 10 Joule
D. 5 Joule
E. 4 Joule
Pembahasan
Diketahui :
Tekanan awal (P1) = 4 Pa = 4 N/m2
Tekanan akhir (P2) = 6 Pa = 6 N/m2
Volume awal (V1) = 2 m3
Volume akhir (V2) = 4 m3
Ditanya : Usaha yang dilakukan oleh gas (W)
Jawab :
Usaha yang dilakukan gas = luasan di bawah kurva a-b.
W = luas segitiga + luas persegi panjang
W = ½ (6-4)(4-2) + 4(4-2)
W = ½ (2)(2) + 4(2)
W = 2 + 8
W = 10 Joule
9.)Suatu gas memiliki volume awal 2,0 m3 dipanaskan dengan kondisi isobaris hingga volume akhirnya menjadi 4,5 m3. Jika tekanan gas adalah 2 atm, tentukan usaha luar gas tersebut!
(1 atm = 1,01 x 105 Pa)
Pembahasan
Data :
V2 = 4,5 m3
V1 = 2,0 m3
P = 2 atm = 2,02 x 105 Pa
Isobaris → Tekanan Tetap
Data :
V2 = 4,5 m3
V1 = 2,0 m3
P = 2 atm = 2,02 x 105 Pa
Isobaris → Tekanan Tetap
W = P (ΔV)
W = P(V2 − V1)
W = 2,02 x 105 (4,5 − 2,0) = 5,05 x 105 joule
W = P(V2 − V1)
W = 2,02 x 105 (4,5 − 2,0) = 5,05 x 105 joule
10.) 2000/693 mol gas helium pada suhu tetap 27oC
mengalami perubahan volume dari 2,5 liter menjadi 5 liter. Jika R = 8,314 J/mol
K dan ln 2 = 0,693 tentukan usaha yang dilakukan gas helium!!
Pembahasan
Data :
n = 2000/693 mol
V2 = 5 L
V1 = 2,5 L
T = 27oC = 300 K
Data :
n = 2000/693 mol
V2 = 5 L
V1 = 2,5 L
T = 27oC = 300 K
Usaha yang dilakukan gas :
W = nRT ln (V2 / V1)
W = (2000/693 mol) ( 8,314 J/mol K)(300 K) ln ( 5 L / 2,5 L )
W = (2000/693) (8,314) (300) (0,693) = 4988,4 joule
W = nRT ln (V2 / V1)
W = (2000/693 mol) ( 8,314 J/mol K)(300 K) ln ( 5 L / 2,5 L )
W = (2000/693) (8,314) (300) (0,693) = 4988,4 joule



